V lednu letošního roku objevili pracovníci Federálního výzkumného centra pro virologii a mikrobiologii (FRCViM) v Rusku další případ nového typu králičího virového hemoragického onemocnění (RVHD). VGBV se projevuje náhle a vede k hromadnému úhynu zvířat. Co je dnes známo o této nemoci, trajektorii jejího šíření, diagnostických metodách a preventivních opatřeních – v přehledu vědců z NIVI v Samaře a Saratově – poboček Federálního centra pro životně důležitou medicínu. Materiál připravily mladší výzkumní pracovníci SamNIVI Anastasia Glazunova a Daria Lunina, ředitelka SamNIVI Olga Kustikova, ředitelka SarNIVI Světlana Konnova, zástupkyně. Ředitel výzkumu SamNIVI Pavel Ilyasov.
V lednu letošního roku objevili pracovníci Federálního výzkumného centra pro virologii a mikrobiologii (FRCViM) v Rusku další případ nového typu králičího virového hemoragického onemocnění (RVHD). VGBV se projevuje náhle a vede k hromadnému úhynu zvířat. Co je dnes známo o této nemoci, trajektorii jejího šíření, diagnostických metodách a preventivních opatřeních – v přehledu vědců z NIVI v Samaře a Saratově – poboček Federálního centra pro životně důležitou medicínu. Materiál připravily mladší výzkumní pracovníci SamNIVI Anastasia Glazunova a Daria Lunina, ředitelka SamNIVI Olga Kustikova, ředitelka SarNIVI Světlana Konnova, zástupkyně. Ředitel výzkumu SamNIVI Pavel Ilyasov.
Virové hemoragické onemocnění králíků (RHD) je akutní, vysoce nakažlivé onemocnění způsobené kalicivirem (rod Lagovirus, čeleď Caliciviriade), postihující králíka evropského (Oryctolagus cuniculus) a charakterizované projevy trombohemoragického syndromu ve všech orgánech, zejména v plicích a játrech. [1–3].
V současné době jsou známy dva sérotypy viru RHD, které se nazývají RHDV a RHDV2 (RHDVb) [4]. Byla popsána řada variant RHDV [5]. Klinický obraz onemocnění způsobeného RHDV a RHDV2 je přitom poněkud odlišný a v závislosti na sérotypu viru, který onemocnění vyvolal, se používají vhodné vakcíny a léčebné metody [6].
Nemoc je spojena s velkými ekonomickými škodami, protože podle současných veterinárních pravidel jsou všichni králíci na nefunkční farmě okamžitě poraženi [1, 3, 4].
Co je o viru známo?
Původcem RHD je neobalený RNA virus. Do rodu Lagovirus patří také virus EBHSV, který způsobuje syndrom zajíce hnědého, onemocnění velmi podobné RHD. Navzdory vysoké genetické podobnosti (identita nukleotidové sekvence genu VP60 je 70 %) jsou RHDV a EBHSV dva různé druhy [4, 7, 8].
Srovnání nukleotidových sekvencí a antigenů, stejně jako epidemiologická data, naznačují existenci tří hlavních skupin RHDV:
1. „Classic RHDV“ se poprvé objevilo v Číně v roce 1984 [9]. Tento virus, registrovaný ve více než 40 zemích Asie, Afriky, Ameriky, Evropy a Oceánie, je dosud endemickým onemocněním ve většině zemí, kde evropští králíci žijí v přirozených podmínkách nebo jsou domestikovaní [4].
2. Subtyp RHDVa/G6, poprvé identifikovaný v Evropě v roce 1996 [10, 11], se nyní rozšířil do dalších částí světa (Oceánie, Asie a Amerika [4]).
3. „Nová“ RHDV (prozatímně označovaná jako RHDV2 nebo RHDVb) se objevila ve Francii v roce 2010 u volně žijících a chovaných očkovaných králíků [12–14] a rychle se rozšířila v Evropě a středomořských oblastech (Malta a Tunisko), jakož i v Austrálie v roce 2015. Podle [13] RHDV2 nepochází z klasického RHDV. Antigenní data umožnila klasifikaci RHDV2 jako druhého sérotypu RHDV [4].
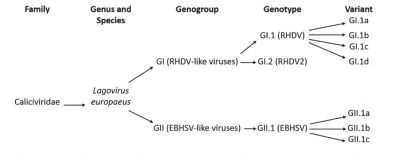
Rýže. 1. Klasifikace patogenních lagovirů [6]
Sérologická studie RHD [15–18] v Itálii identifikovala nepatogenní lagovirus související s RHDV a pojmenovaný RCV. Různí autoři identifikují tento virus jako samostatný druh nebo jej považují za nepatogenní kmen RHDV. Následně byl tento lagovirus zaznamenán v dalších evropských zemích a také v Austrálii a Oceánii [15, 19–23]. Tento virus způsobuje zákeřnou infekci střevního traktu, která není provázena klinickými příznaky, ale vyvolává sérologickou odpověď, která může komplikovat diagnostiku RHD [16, 18, 21, 24, 25].
RHD je vysoce nakažlivá. Experimenty prokázaly přenos orální, nazální, subkutánní, intramuskulární nebo intravenózní cestou, stejně jako mechanický přenos přes mouchy, jiný hmyz a volně žijící zvířata [26].
Zdrojem nákazy jsou nemocní a uzdravení králíci. Zdraví králíci se nakazí především dýchacími cestami, když jsou chováni společně s nemocnými a zotavujícími se zvířaty [27], a také prostřednictvím fomitů, včetně kontaminované potravy, vody a podestýlky. Jednou z hlavních cest přenosu viru do nových oblastí je navíc dovoz kontaminovaného králičího masa a virus přežije i zmrazení.
Virus je perzistentní v prostředí. Jeho virulence se nesníží při působení etheru, chloroformu nebo trypsinu; při zahřívání po dobu 1 hodiny na 50 °C. Patogen je stabilní v rozmezí pH od 4,5 do 10,5; je odolný vůči pH 3,0, ale je inaktivován roztokem formalínu nebo teotropinu nebo při pH>12 [26] a teplotě 4-37 °C během dne. Při teplotě -40°C virus přetrvává déle než pět let [28].
VGBV postihuje divoké a domestikované králíky druhu Oryctolagus cuniculus.
Jiné druhy králíků, včetně Sylvilagus floridanus, Lepus californicus a Romerolagus diazzi, nejsou vnímavé.
Zajíci hnědí (Lepus europaeus) a další druhy zajíců (L. timidus, L. corsicanus, L. capensis) nejsou citlivé na klasické kmeny RHDV/RHDVa.
Virus může infikovat králíky všech věkových kategorií, ale u zvířat mladších 6–8 týdnů je infekce subklinická. Patogenetický mechanismus rezistence k RHD viru klasického antigenního podtypu u mladých zvířat je stále nejasný. U 5–10 % králíků mladších 4–6 týdnů je zaznamenána subakutně-chronická forma RHDV/RHDVa.
Průběh onemocnění u dospělých králíků (nad 40–50 dní) může být hyperakutní, akutní, subakutní nebo chronický.
Hyperakutní RHD je asymptomatická. Zvířata mohou zemřít dva až tři dny po infekci [1, 3].
Klinický obraz se projevuje především akutní infekcí s příznaky jako anorexie, apatie, vyčerpanost, nervové příznaky (křeče, ataxie, paralýza, opistotonus), respirační příznaky (dušnost, pěnivý a krvavý výtok z nosu), cyanóza sliznic . Inkubační doba RHDV/RHDVa se však pohybuje od jednoho do tří dnů a smrt nastává 12–36 hodin po nástupu horečky (> 40 °C) [4, 26].
Subakutní forma se vyznačuje podobnými, ale více vyhlazenými znaky.
Charakteristiky klinického obrazu s RHDV2 jsou následující: úhyn sajících králíků od 15 dnů věku a klinické příznaky se objevují po delší dobu (od tří do pěti dnů). Většina králíků má navíc subakutně-chronické projevy onemocnění. Mortalita na RHDV2 je nižší, ale vysoce variabilní (5 % až 70 %); Mezi experimentálně infikovanými králíky je úmrtnost 20 % [29].
VGBK je nutné odlišit od pasteurelózy, salmonelózy, kolibacilózy, myxomatózy, eimeriózy, otravy, úpalu a úpalu.
Vzorky pro výzkum
Jako vzorky lze použít čerstvá a mražená játra [3], čerstvou slezinu a krev, dále formalizované výše zmíněné orgány, plíce a ledviny [1, 26].
Játra obsahují nejvyšší virový titr (od 10 LD3 do 50 LD10/ml 6% homogenátu), což umožňuje identifikaci RHDV i EBHSV. Množství viru přítomného v jiných částech těla je přímo úměrné jejich vaskularitě [50].
RHDV nelze kultivovat v buněčné kultuře (pro izolaci viru). Onemocnění však může být diagnostikováno detekcí virových nukleových kyselin a/nebo antigenů v tkáních a krvi.
Pro diagnostiku se nejčastěji používá metoda PCR. V současné době byly vyvinuty PCR kity pro všechny podtypy viru. Virovou RNA lze nalézt v mnoha orgánech (zejména v játrech), dále v krvi, moči a stolici. Navíc ji lze zjistit v krvi králíků, kteří se již z nemoci dlouhodobě zotavovali.
Další metody pro detekci virové RNA zahrnují reverzní transkripci-PCR a sekvenování, které jsou popsány v literatuře a jsou často používány ve vědeckém výzkumu.
Virové antigeny jsou často detekovány pomocí ELISA. Tato metoda navíc umožňuje dlouhodobě detekovat protilátky v těle uzdravených králíků.
K detekci RHDV lze také použít elektronovou mikroskopii. Játra nemocného zvířete obsahují vysoký titr viru a velké množství lze nalézt ve slezině a krvi. Při dlouhodobém onemocnění je RHD virus snadněji detekovatelný ve slezině než v játrech.
K diagnostice onemocnění jsou vhodné testy založené na hemaglutinaci, sendvičové ELISA a Western blottingu [4, 26].
RHD byl poprvé objeven v zimě roku 1983 v provincii Jiangsu, Čínská lidová republika [9]. Ohnisko se rozšířilo mezi angorské králíky a během devíti měsíců zabilo 14 milionů zvířat [27].
Virus se do Evropy dostal v roce 1988, kde se rychle rozšířil. V roce 1992 byla nemoc hlášena ve Velké Británii. Koncem 1990. let se RHD rozšířila do 40 zemí a stala se endemickou v populacích divokých zajíců a divokých králíků v Evropě, Austrálii, na Novém Zélandu a na Kubě. Současně v Evropě došlo k rychlému nárůstu objemu výzkumu RHD, což bylo způsobeno naléhavostí problému a velkými ekonomickými ztrátami v chovu králíků [27].
V roce 2010 bylo ve Francii zaznamenáno první ohnisko nového typu viru (RHDV2) [13]. Poté byla ohniska onemocnění způsobené tímto virem zaznamenána v Itálii, Španělsku v roce 2011 a v Portugalsku v roce 2012. Virus byl geneticky i antigenně odlišný od klasického RHD viru a dokázal vůči němu částečně překonat imunitu.
Pokud jde o SSSR, Rusko a sousední země, od roku 1987 je onemocnění zaznamenáno v pěti regionech Ukrajiny (Sumy, Charkov, Kyjev, Záporoží, Oděsa), Bělorusku, Moldavsku, Lotyšsku, Uzbekistánu, Kazachstánu a Turkmenistánu.
V Rusku se VGBK poprvé objevila v roce 1986 na Dálném východě na státní farmě Dalnevostočnyj sousedící s Čínou. Poté specialisté, aniž by diagnostikovali nemoc, okamžitě zabili králíky v masokombinátu Birobidzhan a poslali asi 5 tisíc kůží do továrny na plsti Voskresensk. Odtud se nemoc začala šířit po celém moskevském regionu a dalších regionech Ruska [1]. Do roku 1987 bylo touto nemocí postiženo 31 regionů země.
V roce 2006 byla poprvé objevena varianta podtypu viru RHDVa v oblasti Belgorod v Ruské federaci. Na začátku roku 2010 byla v Saratovské a Kurské oblasti zaregistrována ohniska virového hemoragického onemocnění králíků.
V roce 2014 ohlásilo informační a analytické centrum Rosselchoznadzor vypuknutí RHDV2 v Čeljabinské oblasti. V roce 2018 byl virus RHDV2 izolován z mrtvých králíků v oblasti Tveru a Moskvy [38]. Mapové údaje o ohniscích v těchto regionech jsou uvedeny na obrázku 2.
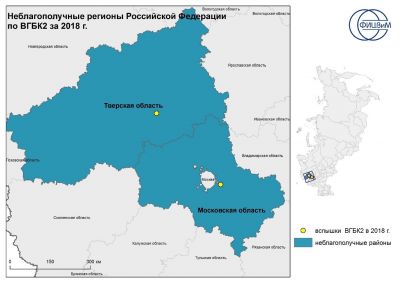
Rýže. 2. Epizootická situace ve světě za posledních pět let podle OIE [39]
V roce 2015 byla ohniska králičího virového hemoragického onemocnění oficiálně potvrzena v Austrálii, Švédsku, Dánsku, Norsku, Beninu (Afrika) a Tunisku.
V roce 2016 bylo podle OIE virové hemoragické onemocnění králíků hlášeno v Dánsku (4), Irsku (2), Norsku (2), Finsku (1), Švýcarsku (4), Švédsku (1), Pobřeží slonoviny (Afrika) (5), Kanada (2), Austrálie (3).
Od roku 2017 byla ohniska RHDV2 hlášena v Austrálii (1), Dánsku (7), Finsku (1), Norsku (2). Situace se dramaticky změnila v roce 2018, kdy bylo zaznamenáno 21 ohnisek RHDV2 v zemích jako Kanada (11), Izrael (8) a Rusko (2). Kromě toho byla na Novém Zélandu (1) identifikována ohniska RHDVa a ve Spojených státech amerických (1). Údaje o celosvětové epidemii za roky 2017–2018. jsou uvedeny na obrázku 3.
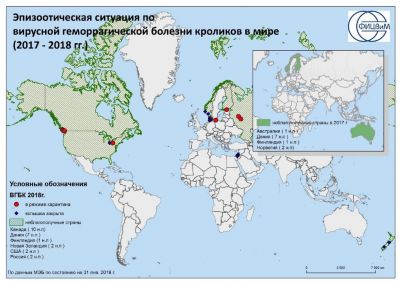
Rýže. 3. Epizootická situace ohledně VGBV ve světě za období od 01.01.2017 do 31.01.2019
Hlavní ekonomické škody pochází z hromadného úhynu zvířat, dosahujícího až 100 %. Velké náklady jsou také spojeny s prováděním omezujících a veterinárních a sanitárních opatření [40].
Léčba a vakcíny
Pro léčbu bylo vyvinuto specifické anti-VGBV sérum, které má terapeutický účinek po jednorázové injekci v objemu 0,5 cm i při rozvoji primárních klinických příznaků onemocnění. Účinnost terapeutického účinku séra v produkčních podmínkách v období epizootiky VGBV se pohybovala od 90 do 97 %.
Aby se předešlo úhynu domácích dekorativních králíků na VGBV, používá se na farmách několik vakcín, které eliminují možné ztráty hospodářských zvířat. Nejběžnější z nich jsou „Pestorin“ (výrobce „Bioveta“, Česká republika), „Hemorrhagivak“ (Bio-Test-Laboratory, Ukrajina), tkáňově inaktivovaná vakcína proti VGBV (Pokrov, Rusko), tkáňově inaktivovaná vakcína proti GBC hliníku hydroxid (Pokrov, Rusko), vakcína proti HBK (vyrábí biofactory Sumy, Ukrajina), inaktivovaná olejová vakcína „Rivak“ (Mevak, Slovensko).
Vzorek vakcíny proti VGBV-2 byl vyroben na FITSVIM a pokračují práce na studiu její účinnosti a bezpečnosti.
Prevence VGBV spočívá v přísném dodržování veterinárních a hygienických pravidel králíkárnami, podniky a soukromými majiteli zvířat. Když se objeví nemoc, farma je prohlášena za nepříznivou a jsou zavedena omezení. Nemocní a podezřelí králíci jsou posíláni na porážku a mrtvoly jsou likvidovány. Zbývající králíci jsou nuceni být očkováni proti VGBV vakcíně bez ohledu na načasování předchozí vakcinace.
Dezinfekce se provádí 5% roztokem chloraminu, 2% roztokem formaldehydu, roztokem chlornanu vápenatého s 5% obsahem aktivního chloru. Králičí kůže ze znevýhodněných chovů se při zpracování dezinfikují. Maso zdravých králíků ze znevýhodněných oblastí se vaří a prodává ve znevýhodněném správním území.
Důležité podmínky pro zabránění šíření VGBV:
1. Včasné informování majitelů o nemoci.
2. Dodržování a zlepšování opatření biologické bezpečnosti na farmách.
3. Monitoring u divokých králíků a zajíců, analýza rizik.
4. Aby se zabránilo šíření VGBV2, je nutné dokončit a zaregistrovat vakcínu a připravit lék pro hromadnou výrobu.
















